اسپوندیلیتِ محوری (axSpA) یکی از مهمترین عللِ «درد کمرِ التهابی» در افراد جوان و میانسال است؛ اما بهعلت شباهت با کمردردهای مکانیکی، سالها میتواند از دید پنهان بماند و به محدودیتِ تحرک، افت کیفیت زندگی و پیشرویِ ساختاری بینجامد. شناساییِ زودهنگامِ الگوی بالینی، تمایز آن از درد مکانیکی و ورود به مسیر تشخیصِ هدفمند، کلیدِ جلوگیری از عوارضِ بلندمدت است.
در axSpA، درد بهتدریج آغاز میشود، با استراحت بدتر و با فعالیت بهتر میگردد، نیمهٔ دومِ شب بیمار را بیدار میکند و معمولاً به NSAID پاسخِ چشمگیر میدهد. همزمان، ممکن است تظاهراتِ خارجمفصلی مانند یووئیتِ قدامی، پسوریازیسِ پوست/ناخن یا IBD (کرون/کولیت) دیده شود که در انتخابِ درمانِ سیستمیک نقش تعیینکننده دارند.
پاتوفیزیولوژیِ بیماری از برهمکنش ژنتیک (بهویژه HLA-B27)، محورهای التهابی مانند TNF و IL-17 و مفهوم «ارگانِ انتز» شکل میگیرد؛ جایی که التهاب در محلِ اتصالِ تاندون/لیگامان به استخوان به درد، ادمِ مغزِ استخوان در MRI و در نهایت استخوانسازیِ جدید میانجامد. همین زیستشناسیِ بیماری، مبنای کارآمدیِ درمانهای هدفمندِ ضد-TNF، ضد-IL-17 و مهارکنندههای JAK را توضیح میدهد.
رویکردِ مدرن بر اصلِ Treat-to-Target استوار است: سنجشِ منظمِ فعالیت بیماری با شاخصهایی مانند ASDAS-CRP، هدفگذاری برای «فعالیتِ کم یا غیرفعال»، و تعدیلِ درمان تا دستیابیِ پایدار به این هدف. این راهبرد با توانبخشیِ ساختارمند (کششهای اختصاصی، تقویت عضلات مرکزی و تمرینهای تنفسی)، ترک سیگار و اصلاحِ ارگونومی همراه میشود تا درد، ناتوانی و سرعتِ پیشروی کاهش یابد.
این مقاله در مجلهٔ روماتولوژیِ پزشکم با زبانِ روشن اما علمی، نقشهٔ راهِ کامل از «شکِ بالینی» تا «تأییدِ تشخیص» را ارائه میکند: معیارهای ASAS، نقشِ MRI مفاصلِ ساکروایلیاک، جایگاهِ HLA-B27، الگوریتمِ درمان از NSAID تا داروهای هدفمندِ دامنه-محور، مدیریتِ تظاهراتِ خارجمفصلی، ایمنی و واکسیناسیون، و نکاتِ عملیِ پایش و کاهشِ درمان. خواننده—چه پزشکِ عمومی و فیزیوتراپیست باشد و چه بیمار/مراقب—با مطالعهٔ این راهنما میتواند با دیدی ساختاریافته، از تشخیصِ دیرهنگام پرهیز کند و درمانی مؤثر، ایمن و شخصیسازیشده را پی بگیرد.
هشدار پزشکی: این مطلب آموزشی است و جایگزین ارزیابی و درمان پزشک نیست. در صورت بروز علائمی مانند تب بالا، درد کمر همراه با بیاختیاری ادرار/مدفوع، ضعف پیشروندهٔ اندامها، درد قفسهٔ سینه یا تنگی نفس، و همچنین درد/قرمزی چشم با کاهش دید، فوراً به اورژانس مراجعه کنید.
چرا «درد کمر التهابی» کلید تشخیص زودهنگام است؟
کمردرد شایعترین شکایت اسکلتی–عضلانی است اما تنها بخشی از آن منشأ التهابی دارد. «درد کمر التهابی» (IBP) معمولاً زیر ۴۰–۴۵ سال آغاز میشود، تدریجی و مزمن است (> ۳ ماه)، با استراحت بدتر و با فعالیت بهتر میشود، بیمار را در نیمهٔ دوم شب بیدار میکند و به NSAID پاسخ برجسته میدهد. تمایز IBP از کمردرد مکانیکی، مسیر تشخیصی را به MRI، HLA-B27 و معیارهای ASAS هدایت میکند.
جدول ۱. مقایسهٔ درد کمر التهابی و مکانیکی
| ویژگی | التهابی (IBP) | مکانیکی |
|---|---|---|
| سن شروع | زیر ۴۰–۴۵ سال | هر سنی (اغلب پس از فعالیت/آسیب) |
| سیر | تدریجی، مزمن (> ۳ ماه) | حاد/زیرحاد، اغلب با محرک مشخص |
| استراحت/فعالیت | بدتر با استراحت، بهتر با حرکت | بهبود با استراحت، تشدید با فعالیت |
| درد شبانه | شایع (نیمهٔ دوم شب) | غیرشایع |
| پاسخ به NSAID | خیلی خوب طی ۴۸–۷۲ ساعت | متغیر/محدود |
پاتوفیزیولوژی: HLA-B27، محور IL-17 و «ارگانِ انتز»
axSpA از برهمکنش ژنتیک، ایمنی و محیط ناشی میشود. آلل HLA-B27 خطر ابتلا را بالا میبرد و پدیدههایی مانند misfolding و ارائهٔ پپتیدهای التهابزا مطرح است. سیتوکینهای TNF و IL-17A/F در پایداری التهاب نقش محوری دارند و هدف درمانهای بیولوژیک قرار گرفتهاند. مفهوم «ارگانِ انتز» توضیح میدهد چرا التهابِ محل اتصالِ تاندون/لیگامان به استخوان میتواند همزمان درد، ادم مغز استخوان در MRI و در نهایت استخوانسازیِ جدید ایجاد کند. محور روده–مفصل و تغییرات میکروبیوم نیز به تداوم التهاب کمک میکنند.
طیف تظاهرات: محوری، محیطی و خارجمفصلی
محوری
درد لگن/کمر التهابی، خشکی صبحگاهی، محدودیت حرکت ستون فقرات و حساسیت مفاصل ساکروایلیاک شایعاند. درگیری دنده–ستون (costovertebral) میتواند ظرفیت تنفسی را کم کند و در معاینه، کاهش «اکسپنشن قفسهٔ سینه» دیده میشود.
محیطی
انتزیت (پاشنه، توبروزیته تیبیا، اپیکوندیل)، داکتیلیت و آرتریت محیطی—بهویژه زانو/مچ—ممکن است همراه شوند. وجود دامنهٔ محیطی بر انتخاب درمان اثرگذار است (مثلاً سودمندی سولفاسالازین در فنوتیپ محیطی).
خارجمفصلی
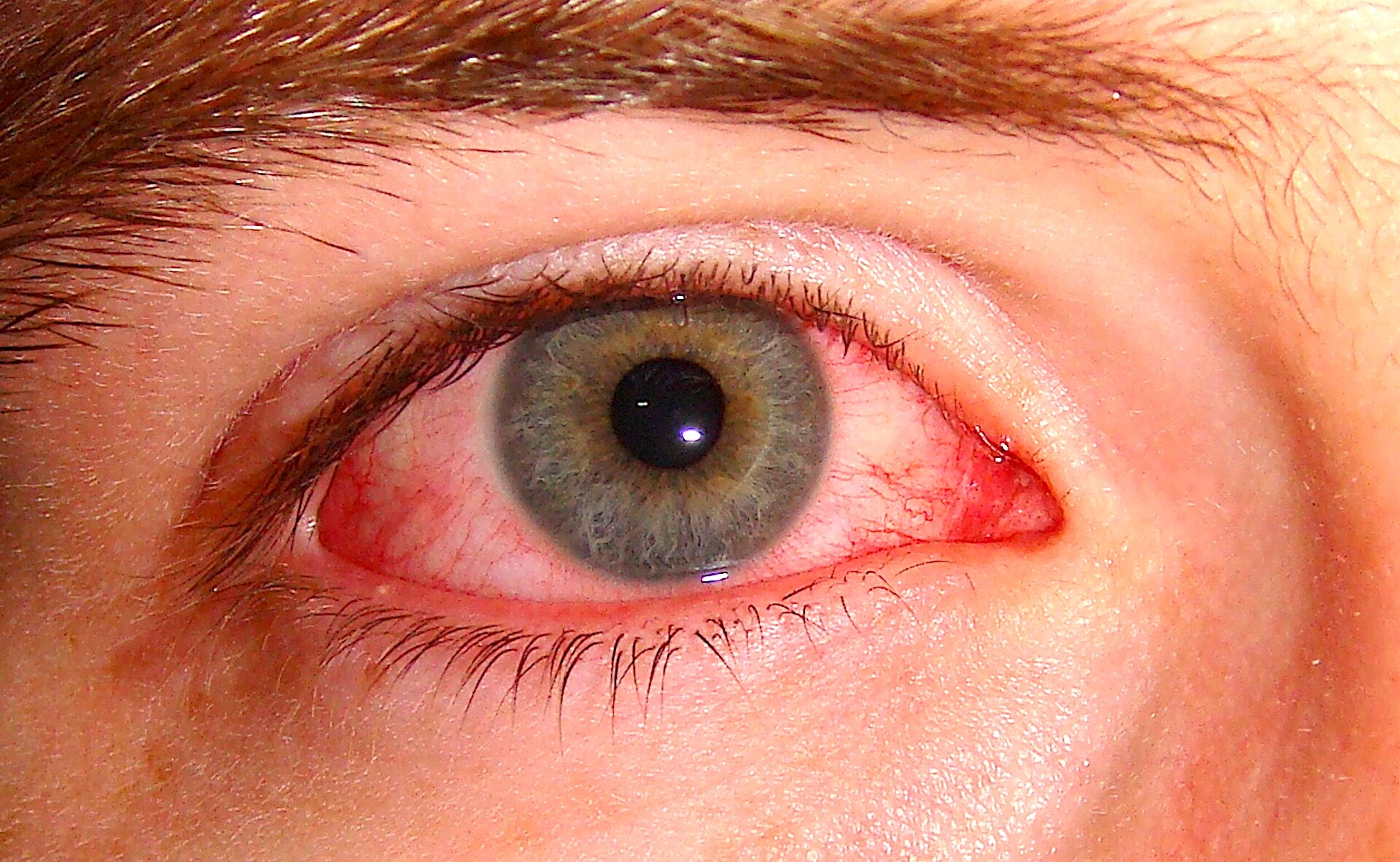
یووئیت قدامی حاد (درد/فتوفوبی/کاهش دید)، پسوریازیس پوستی/ناخن و IBD (کرون/کولیت) از مهمترینها هستند. انتخاب کلاس دارویی باید با این همبودیها همسو باشد: در IBD فعال، TNF مونوکلونال نسبت به IL-17 ارجح است؛ در پسوریازیس شدید، مهار IL-17 گاهی کاراتر است؛ در یووئیت، TNF مونوکلونال بر اتانرسپت برتری دارد.
رویکرد تشخیصی: از شک بالینی تا تأیید
مرحلهٔ اوّل: شناسایی IBP و رد «پرچمهای قرمز»
در هر کمردرد مزمنِ زیر ۴۵ سال، به IBP بیاندیشید. همزمان، پرچمهای قرمز مانند سرطان/عفونت/شکستگی/سندروم دماسبی را رد کنید (تب، کاهش وزن، نقص عصبی پیشرونده، تروما).
مرحلهٔ دوم: آزمایشها
CRP/ESR میتوانند بالا باشند اما طبیعی بودن آنها بیماری را رد نمیکند. HLA-B27 ارزش افزودهٔ تشخیصی دارد، اما مثبت بودن بهتنهایی تشخیص نیست و باید در بسترِ کلینیکی/تصویربرداری تفسیر شود.
مرحلهٔ سوم: تصویربرداری
رادیوگرافی لگن میتواند «ساکروایلیت» ساختاری را در r-axSpA نشان دهد، اما در مراحل اولیه حساس نیست. MRI STIR مفاصل ساکروایلیاک برای التهاب فعال (ادم مغز استخوان) کلیدی است؛ تفسیر باید با احتیاط انجام شود، چون ورزشِ شدید، زایمان و برخی حالات میتوانند یافتههای کاذب بسازند. در ستون فقرات، ضایعات Romanus و التهاب زوائد ممکن است دیده شود.
مرحلهٔ چهارم: معیارهای ASAS—طبقهبندی، نه تشخیص
معیارهای ASAS برای پژوهش طراحی شدهاند ولی در بالین راهگشا هستند. شرط پایه «کمردرد مزمنِ زیر ۴۵ سال» است؛ سپس یکی از دو بازوی «تصویربرداری» یا «بالینی» برای طبقهبندی برآورده میشود.
جدول ۲. روساخت معیارهای ASAS برای axSpA (خلاصهٔ کاربردی)
| بازو | مولفهٔ لازم | سایر الزامات | نکته |
|---|---|---|---|
| تصویربرداری | MRI مثبت SIJ یا ساکروایلیت رادیوگرافیک | حداقل یک ویژگی اسپوندیلوآرتریت (HLA-B27، IBP، یووئیت، پاسخ عالی به NSAID، سابقهٔ خانوادگی، CRP بالا، پسوریازیس، IBD و…) | حساس برای تشخیص زودهنگام |
| بالینی | HLA-B27 مثبت | حداقل دو ویژگی اسپوندیلوآرتریت از فهرست بالا | وقتی MRI منفی/در دسترس نیست |
اندازهگیریِ فعالیت و هدفگذاری: ASDAS در مرکز توجه
ASDAS-CRP شاخص ترجیحی فعالیت بیماری در axSpA است. آستانههای پرکاربرد: < ۱٫۳ (بیماری غیرفعال)، < ۲٫۱ (فعالیت کم)، ۲٫۱–۳٫۵ (فعالیت بالا) و > ۳٫۵ (خیلی بالا). راهبرد Treat-to-Target دستیابی پایدار به «بیماری غیرفعال یا کمفعال» را هدف میگیرد و تصمیمهای افزایشی/تعویض دارو را هدایت میکند.
جدول ۳. شاخصها و پایش دورهای
| شاخص/آزمایش | کاربرد | فراوانی پیشنهادشده | هدف/توضیح |
|---|---|---|---|
| ASDAS-CRP | فعالیت بیماری (ترجیحی) | هر ۶–۱۲ هفته در اینداکشن؛ سپس هر ۳–۶ ماه | هدف: < ۲٫۱؛ ایدهآل: < ۱٫۳ |
| BASDAI | شاخص مبتنی بر گزارش بیمار | همزمان با ASDAS | آستانهها در زمینهٔ بالینی تفسیر شوند |
| BASFI/BASMI | کارکرد/تحرک | هر ۶–۱۲ ماه | پایش طولی توان عملکردی/تحرک |
| CRP/ESR | التهاب سیستمیک | با هر ارزیابی ASDAS | CRP در همهٔ بیماران بالا نیست |
مدیریت چندلایه: از توانبخشی تا درمان هدفمند
غیردارویی (ستونِ فراموشنشدنی)
آموزش بیمار، ترک سیگار، مدیریت وزن، بهداشت خواب و ورزش ساختارمند (کششهای زنجیرهٔ خلفی، تمرینهای قدرتی عضلات مرکزی، تمرینهای تنفسی برای بهبود اکسپنشن) اساس مدیریتاند. برنامهٔ فیزیوتراپی و تمرینات خانگی نسخهشده، درد و ناتوانی را کاهش میدهند. آبدرمانی و تمرین در آب گرم، سفتی و درد را کم میکند.
NSAID (خط اول دارویی)
NSAIDها خط اول داروییاند. توصیه میشود دو NSAID متفاوت را هر کدام با دوز کافی و مدت کوتاه ارزیابی کنید. مصرف مداوم در برخیِ پرخطرانِ پیشروی ساختاری مطرح شده، اما توازن خطرات قلبی–گوارشی باید سنجیده شود. مهارکنندههای COX-2 برای افراد با خطر خونریزی گوارشی گزینهای هستند ولی خطر قلبی–عروقی را نباید نادیده گرفت.
گلوکوکورتیکوئید
کورتون سیستمیک برای محورِ مزمن توصیه نمیشود. تزریق موضعی تحت هدایت تصویربرداری در مفصل ساکروایلیاک/انتزِ منفرد میتواند مفید باشد؛ تکنیک آسپتیک ضروری است.
csDMARDها
سولفاسالازین در فنوتیپِ «محیطی غالب» (آرتریت محیطی) میتواند مفید باشد؛ اما روی محور ستون–لگن اثر قانعکنندهای ندارد. متوترکسات برای محور نقشی ثابتشده ندارد.
بیولوژیکها: TNF و IL-17 (و دوگانهٔ IL-17A/F)
در عدم کنترل با NSAID (و با توجه به یافتههای بالینی/تصویربرداری)، آغاز درمان هدفمند منطقی است. مهارکنندههای TNF (آدالیموماب، اینفلیکسیماب، گولیموماب، سرتولیزوماب، اتانرسپت) و مهارکنندههای IL-17A (سکوکینوماب، ایکسکیزوماب) ستونهای اصلیاند. بیمکیزوماب (مهار دوگانهٔ IL-17A/F) در اروپا برای axSpA تأیید شده و کارایی قوی نشان داده است. انتخاب کلاس باید دامنه-محور و همبودی-آگاه باشد: IBD فعال → TNF مونوکلونال؛ پسوریازیس/ناخن شدید → IL-17/بیمکیزوماب؛ یووئیت مکرر → TNF مونوکلونال.
مهارکنندهٔ JAK
اوپاداسیتینیب (JAK-1) برای AS و nr-axSpA تأیید شده است و در بیماران ناکامی/عدم تحمل بیولوژیکها یا ترجیح خوراکی قابل بررسی است. غربال سل نهفته و HBV، پایش عفونت، خطر زوستر و ارزیابی ریسک قلبی–عروقی/ترومبوآمبولی ضروریاند.
جدول ۴. درمانهای هدفمند: انتخاب دامنه-محور و نکات ایمنی
| کلاس/نمونهها | قوتها | محدودیتها/هشدارها | وقتی ارجح است |
|---|---|---|---|
| TNF (آدالیموماب، اینفلیکسیماب، گولیموماب، سرتولیزوماب، اتانرسپت) | اثر وسیع محوری/محیطی؛ دادهٔ طولانیمدت | غربال TB/HBV؛ اتانرسپت در یووئیت/IBD کمتر کاراست | IBD فعال، یووئیت مکرر (TNF مونوکلونال) |
| IL-17A (سکوکینوماب/ایکسکیزوماب) و IL-17A/F (بیمکیزوماب) | اثر عالی بر محور و پوست/ناخن | احتیاط در IBD؛ احتمال کاندیدیازیس مخاطی | پسوریازیس/ناخن شدید، محور غالبِ محوری |
| JAK-i (اوپاداسیتینیب) | خوراکی؛ کارایی در AS و nr-axSpA | ریسک عفونت (زوستر)، ارزیابی خطر قلبی–عروقی/VTE | پس از ناکامی/عدم تحمل بیولوژیک یا ترجیح بیمار |
الگوریتم عملی درمان (تصمیمگیری فردمحور)
قدم ۱: تأیید axSpA و ارزیابی شدت/دامنه
IBP + ویژگیهای SpA + شواهد تصویربرداری/سرولوژی. خط پایه را با ASDAS-CRP، BASDAI، CRP، معاینهٔ حرکتی و ارزیابی تظاهرات خارجمفصلی ثبت کنید.
قدم ۲: آغاز درمان
شروع توانبخشی و NSAID خط اول. در فنوتیپ محیطیِ غالب، افزودن csDMARD قابل بررسی است. در پاسخ ناکافی یا التهاب فعالِ واضح، آغاز بیولوژیک (TNF یا IL-17) بر اساس دامنه/همبودیها؛ JAK-i برای سناریوهای منتخب.
قدم ۳: Treat-to-Target
ارزیابی ASDAS در ۶–۱۲ هفته. در ASDAS ≥ ۲٫۱ یا نبود پاسخ بالینی، افزایش/تعویض دارو (درونکلاس یا بینکلاس). پس از تثبیت بهبود، تاپر محتاطانه (افزایش فاصلهٔ تزریق/کاهش دوز طبق برچسب) قابل بررسی است؛ قطع ناگهانی توصیه نمیشود.
تصویربرداری: از تشخیص تا پایش
MRI SIJ (توالی STIR برای التهاب و T۱ برای ضایعات ساختاری مانند erosion و fat metaplasia) ابزار کلیدی تشخیص زودرس است. در پیگیری، MRI را هنگام تغییر بالینی، نیاز به تصمیم درمانی یا شک به تشخیص تکرار کنید. رادیوگرافی لگن برای ارزیابی پیشروی ساختاری در فواصل بلندتر (مثلاً هر ۲–۳ سال) مفید است.
جدول ۵. تصویربرداریِ axSpA—چه زمانی و چرا؟
| روش | نقش | نکات کلیدی |
|---|---|---|
| MRI SIJ (STIR/T۱) | تشخیص زودهنگام، ارزیابی التهاب/آسیب | یافتههای کاذب پس از زایمان/ورزش ممکن است؛ تفسیر در زمینهٔ بالینی |
| رادیوگرافی لگن | تشخیص ساکروایلیت ساختاری (r-axSpA/AS) | حساسیت کم در مراحل اولیه |
| MRI ستون فقرات | در درد محوری غیرقابل توضیح/شک بالا | سناریو-محور، نه روتین |
همبودیها، ایمنی و پیشگیری
پیش از بیولوژیک/JAK-i غربال سلِ نهفته و HBV/HCV لازم است. واکسیناسیونهای غیرفعال (آنفلوانزا، پنوموکوک) بهروز شود؛ از واکسنهای زنده طی درمان هدفمند پرهیز گردد. خطر پوکی استخوان، بیماری قلبی–عروقی، اختلال خواب و افسردگی را فعالانه پایش کنید. برای یووئیت، «برنامهٔ اقدام چشمی» (درد/قرمزی/فتوفوبی → ارجاع فوری چشم) به بیمار آموزش داده شود.
جمعیتهای ویژه: بارداری، جراحی، شغل و ورزش
در بارداری، NSAID در سهماههٔ سوم ممنوع است؛ برخی TNFها با زمانبندی قطع/ادامه قابل استفادهاند (تصمیم مشترک با زنان/روماتولوژی). پیش از جراحی ستون/لگن، برنامهٔ توانبخشی و قطع/ازسرگیری درمان هدفمند طبق پروتکلهای عفونت/ترمیم زخم هماهنگ شود. در شغلهای سنگین، مداخلات ارگونومیک و تمرینهای محافظ ستون توصیه میشود. ورزشهای هوازی کمضربه (شنا/دوچرخه ثابت) و تمرینهای کششی/قدرتی تدریجی ایمن و مفیدند.
افتراقهای دشوار: چه چیزهایی «شبیه axSpA» بهنظر میرسند؟
کمردرد مکانیکی مزمن، دردهای منشأ دیسک/فاست، هیپرلاگزیتی، سندروم درد میوفاسیال، عفونتهای مهره (اسپوندیلودیسکیت)، بدخیمیها و استئوآرتریت SI میتوانند تقلیدگر باشند. MRI و الگوبرداری دقیق علائم، بههمراه پاسخ به NSAID، افتراق را آسانتر میکند. در ورزشکاران حرفهای/پس از زایمان، یافتههای MRI را با احتیاط تفسیر کنید.
خطاهای رایج و دامهای مدیریتی
- اتکا به NSAID بلندمدت بدون راهبرد Treat-to-Target و بدون پایش ASDAS؛ نتیجهٔ آن تداوم درد/ناتوانی و خطر پیشروی ساختاری است.
- انتخاب کلاس هدفمند بدون توجه به تظاهرات خارجمفصلی (مثلاً انتخاب IL-17 در IBD فعال یا اتانرسپت در یووئیت مکرر) و نادیدهگرفتن غربال عفونت نهفته پیش از درمان.
نکات عملی برای کلینیکهای شلوغ
- از ویزیت اول «پروفایل پایه» بسازید: ASDAS-CRP، BASDAI، CRP، دامنهٔ حرکتی، اکسپنشن قفسهٔ سینه و نسخهٔ تمرین خانگی.
- در هر نوبت یک «هدف ملموس» تعیین کنید: مثلاً کاهش ASDAS به زیر ۲٫۱ در سه ماه و سپس تلاش برای < ۱٫۳.
مطالعهٔ بیشتر (PDF/رسمی)
۱) ASAS-EULAR ۲۰۲۲ — توصیههای مدیریت اسپوندیلیت محوری (نسخهٔ کامل PDF):
دانلود PDF
۲) ACR/SAA/SPARTAN ۲۰۱۹ — راهنمای درمان AS و nr-axSpA (نسخهٔ آزاد):
دانلود PDF
۳) معیارهای طبقهبندی ASAS برای axSpA — مقالهٔ اصلی ۲۰۰۹:
دانلود PDF
۴) آستانههای ASDAS و حالتهای فعالیت — دادهٔ تکمیلی J Rheumatol ۲۰۲۴:
دانلود PDF
جمعبندی
اسپوندیلیت محوری بیماریای قابل هدفگیری است: تشخیص زودهنگامِ درد کمر التهابی، استفادهٔ دقیق از MRI/HLA-B27 و معیارهای ASAS، آغاز بهموقع توانبخشی و NSAID، و سپس درمان هدفمند دامنه-محور (TNF/IL-17/JAK) با راهبرد Treat-to-Target، کیفیت زندگی و عملکرد را بهطور معناداری بهبود میدهد و خطر پیشروی ساختاری را کاهش میدهد. پایش منظم ASDAS، تصمیمهای تعویض/تکمیل درمان را منطقی میکند؛ توجه همزمان به همبودیها و ایمنی (غربال عفونت، واکسیناسیون، سلامت استخوان/قلب) لازمهٔ درمان موفق بلندمدت است.
کلمات کلیدی: اسپوندیلیت محوری، درد کمر التهابی، AS، nr-axSpA، ASAS، MRI، HLA-B27، ASDAS، Treat-to-Target، TNF، IL-17، اوپاداسیتینیب.